Prophylaxe in Neutropenie: Posaconazole vs Fluconazole / Itraconazole
Die Frage nach dem prophylaktischen Einsatz eines Antimykotikums bei Patienten in Neutropenie bleibt mit der Einführung von Posaconazole wohl weiterhin umstritten.
Die prophylaktische Gabe eines Antimykotikums bei Patienten in Neutropenie wird bisher unterschiedlich gehandhabt: Befürworter streichen die Schwierigkeit der frühzeitigen Diagnose einer invasiven Mykose und die hohe Mykose-assoziierte Mortalität heraus. Gegner heben die mangelnde Evidenz der Mortalitätsreduktion unter Fluconazole (was nicht zuletzt an der pharmakologisch bedingten geringgradigeren Wirksamkeit gegen Schimmelpilze liegen dürfte), die eingeschränkte Verträglichkeit von Itraconazole und die Bildung von Resistenzen hervor. Unumstritten ist der Erfolg einer Fluconazole-Prophylaxe bei Patienten mit allogenen Stammzell-Transplantationen. Die im NEJM erschienene, doppelblind randomisierte Multizenter-Studie (89 Zentren weltweit) untersucht den Erfolg einer Prophylaxe bei Patienten mit AML oder MDS. Die vergleichenden Substanzen sind Posaconazole, welches sich durch ein breites Spektrum (Sprosspilze, Schimmelpilze und Mucorales) auszeichnet versus Fluconazole (keine Wirkung gegen Schimmelpilze und Mucorales) und Itraconazole (mässiggradige Wirksamkeit gegen Schimmelpilze, kaum wirksam gegen Mucorales).
Untersucht wurden 602 Patienten mit neuer Diagnose oder erstem Rezidiv einer AML oder eines MDS ab dem 14. Lebensjahr mit einer voraussichtlichen Dauer der Neutropenie während mindestens 7 Tagen. Gemäss lokaler Praxis wurde peroral mit Fluconazole (400mg/d, 240 Patienten) oder Itraconazole (2x200mg/d 58 Patienten) respektive mit verblindetem Posaconazole (3x200mg/d, 304 Patienten) therapiert. Die Prophylaxe wurde zu jedem Chemotherapiezkylus gegeben, entweder ab 24h nach der letzten Anthracyclindosis oder ab erstem Tag der Chemotherapie. Die Dauer betrug je nach dem, was zuerst eintraf: Erholung der Neutropenie, Auftreten einer invasiven Mykose, komplette Remission oder bis 12 Wochen ab 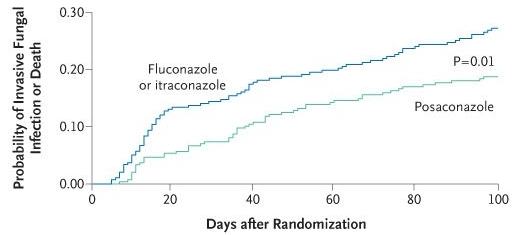 Randomisation mit follow up 30 Tage nach letzter Gabe eines Antimykotikums und bis 100 Tage nach Randomisation. Das Monitoring umfasste regelmässige Galactomannan-Untersuchungen und Blutkulturen im Falle von Zeichen einer Infektion. Primärer Endpunkt waren die Inzidenz vermuteter oder bewiesener invasiven Mykosen während der Gabe der Prophylaxe. Sekundäre Endpunkte stellten die Inzidenz invasiver Pilzinfektionen innert 100 Tage nach Randomisation und die Untersuchung eines Behandlungserfolgs während der Behandlungsphase dar.
Randomisation mit follow up 30 Tage nach letzter Gabe eines Antimykotikums und bis 100 Tage nach Randomisation. Das Monitoring umfasste regelmässige Galactomannan-Untersuchungen und Blutkulturen im Falle von Zeichen einer Infektion. Primärer Endpunkt waren die Inzidenz vermuteter oder bewiesener invasiven Mykosen während der Gabe der Prophylaxe. Sekundäre Endpunkte stellten die Inzidenz invasiver Pilzinfektionen innert 100 Tage nach Randomisation und die Untersuchung eines Behandlungserfolgs während der Behandlungsphase dar.
Vermutete oder bewiesene invasive Mykosen traten während der Behandlung mit 2% in der Posaconazole-Gruppe signifikant geringer als in den Vergleichsgruppen mit 8% auf. Innert dem Beobachtungszeitraum von 100 Tagen stiegen die invasiven Mykosen in der Posaconazolegruppe auf 5%, in den Vergleichsgruppen auf 11% an. Das Auftreten bis zur invasiven Mykose betrug in der Posaconazolegruppe 41+- 26 Tage, in den Vergleichsgruppen 25+-26 Tage. Aspergillus war der am meiste nachgewiesene Keim zugunsten der Fluconazole- / Itraconazole-Gruppe, wobei die Mehrheit der Nachweise mittels Galctomannan-Antigen erfolgte. 22% der Posaconazole-Gruppe und 34% der Vergleichsgruppen bedurften einer empirischen antifungalen Therapie (beispielsweise mittels Amphotericin B, im Paper selbst nicht weiter aufgeschlüsselt) während mindestens 4 Tagen. Die Gesamtmortalität während der Behandlungsdauer war mit einem p = 0.048 nur knapp signifikant: in der Posaconazole-Gruppe verstarben 16% versus 22% der Vergleichsgruppen (signifikanterer Unterschied mit 14% vs. 21% innert der Beobachtungszeit von 100 Tagen, effektive Mortalitätsreduktion der Posaconazole-Gruppe zu 33% mit einer NNT von 14 Patienten im Vergleich zur Fluconazole- / Itraconazolegruppe). Die auf Pilzinfektionen zurückgeführte Mortalität betrug in der Posaconazole-Gruppe 2% versus 5% in der Fluconazol- / Itraconazolgegruppe (p=0.01).
Relevante Nebenwirkungen traten in der Posaconazole-Gruppe mit 6% versus 2% der Fluconazole- oder Itraconazole-Gruppe signifikant häufiger auf (p= 0.01) und umfassten QTc-Verlängerungen (bei einem Patient der Posaconazole-Gruppe "serious"), Vorhofflimmern, Verminderung der Auswurffraktion, torsade de pointes (jeweils in der Posaconazole-Gruppe).
Die Autoren schliessen auf einen möglichen Nutzen der Prophylaxe mittels Posaconazole. Es bleibt kritisch anzumerken, dass ein Vergleich respektive Rückschluss der Mortalität mit einer Placebo-Gruppe fehlt, die angegebenen Diagnosen invasiver Aspergillosen vornehmlich auf dem Galactomannan-Antigen-Test (und deutlich weniger auf dem kulturellen Wachstum) beruhen. Die Interpretation der Mortalitätsrate wird zudem dadurch erschwert, dass in beiden Gruppen beträchtliche Anteile eigentliche empirische antifungale Therapien erfuhren. Zudem ist anzulasten, dass die Mortalitätsberechnungen der Itraconazole- und Fluconazole-Gruppe gemeinsam und nicht subanalysiert gezeigt werden – kann doch erwartet werden, dass aufgrund eines breiter abgedeckten Spektrums mit Itraconazole die Mortalität und vor allem der Unterschied zur Posaconazole-Gruppe geringer ausfallen könnte. Im in der gleichen Ausgabe erschienen Editorial wird zudem angeprangert, dass der eigentliche evidenzbasierte Wirknachweis von Posaconazole gegen invasive Aspergillosen im klinischen Alltag noch aussteht. Und last but not least bleibt zu hinterfragen, welche Resistenzbildungen in Kauf genommen werden, wenn mit einem Antimykotikum mit breitem Spektrum eine systematische Prophylaxe betrieben wird.
Quelle: N Engl J Med 2007;356:348-59