HPV-assoziierte Tumoren
HPV-Assoziation ist bei einer grossen Zahl von Tumoren bekannt und beträgt bei Zervix-Ca 100%, Analkrebs 86%, Tumoren des Oropharynx 55% und Karzinomen von Vulva/Vagina bzw. Penis um 30%.
Inzidenz von Zervixkarzinom mit und ohne HIV-Therapie
Weltweit sind Morbidität und Mortalität wegen Zervixkarzinom unter HIV-positiven Frauen enorm. Dies betrifft vor allem Länder, in denen Screening nicht fest etabliert ist. In Subsahara-Afrika ist es der häufigste Grund für Krebstod bei HIV-positiven Frauen. Dabei führt HIV zu einer erhöhten Progressions- und verminderten Regressionsrate der Dysplasien bei HIV-positiven Frauen. Sie erkranken oft sehr jung.
In der Schweizer Kohorte (Abstr 730) und einer Studie aus Botswana (Abstr 731) hatte sich keine (signifikante) Reduktion unter ART bzw. sogar ein Zuwachs gezeigt.
Blinde Biopsie erhöht Diagnoserate für Analkrebs 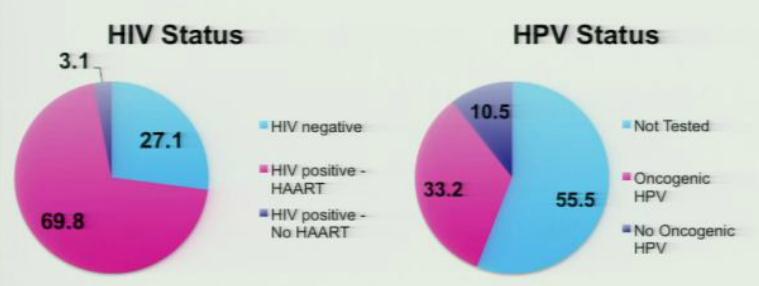
Beim Zervixkarzinom ist bekannt, dass „Zufallsbiopsien“ (an inspektorisch unauffälligen Arealen zufällig entnommene Biopsien) in mehr als 1/3 deutliche Auffälligkeiten zeigen. Gilt dies auch für den Analkanal?
R. Silvera, New York, zeigte Daten von 391 Patienten mit hochauflösender Anoskopie. 70% wurden wegen abnormer analer Zytologie zugewiesen. Wie Bild rechts zeigt, handelte sich um ein recht heterogenes Kollektiv.
Aus total 253, bei der Anoskopie verdächtig aussehenden Arealen wurden 878 Biopsate entnommen. Diese ergaben in 25% Nachweis von AIN II/III. Zusätzlich wurde 883 mal in vom Untersucher als unauffällig eingestuften Arealen biopsiert. Darin fand sich in 3.7% Nachweis von AIN II/III. Damit wurden 13% aller AIN II/III lediglich aufgrund der Zufallsbiopsien diagnostiziert, d.h. bei 10% aller Patienten wäre falsch von einem unauffälligen Befund ausgegangen worden. Einschränkend kann ein Bias durch mögliche Fehlbeurteilung seitens des Untersuchers trotz teilweiser Resultatüberprüfung nicht ausgeschlossen werden.
Die Diskussion rund um das Screening auf Analkrebs-Vorstufen ist bereits kompliziert. Es stellen sich Fragen zur effizientesten Screeningmethode (zuerst anale Zytologie oder direkt Vorstellung zur Anoskopie mit Biopsie?). Es fehlen zudem ausreichende Daten zur besten Behandlungsmethoden von AIN II/III.
Sollte sich das vorgestellte Studienergebnis (vorzugsweise bei einem reinen HIV-Kollektiv) bestätigen, wäre eine Erweiterung der Biopsien auf normal erscheinende Areale zu diskutieren, allerdings unter Beachtung von Kosteneffektivität und der durch die erhöhte Zahl von Biopsien möglicherweise erhöhten Morbidität.
HPV-Impfung
E. Chiao wies auf ACTG-Daten über die gute Verträglichkeit und Immunogenität der HPV-Impfung auch bei HIV-PatientInnen hin (Kojic A5240). Die meisten Patienten dürften mit den HPV-Viren, gegen welche die Impfung wirkt, bereits vor oder mit Zeitpunkt der HIV-Infektion Kontakt gehabt haben. Somit kommt die Impfung zur Primärprävention zu spät.
Gemäss E. Chiao führt eine HPV-Impfung auch nicht zu rascherer Ausheilung einer HPV-Infektion oder einer Dysplasie. Dennoch gibt es bei HIV-Infektion interessante, innovative Anwendungsbereiche der HPV-Impfung: eine Studie hatte nach operativer CIN-Behandlung bei vorheriger HPV-Impfung eine um 65% tiefere Inzidenz von CIN als nach Placeboimpfung beobachtet (Joura BMJ 12). Dies wurde auch bei Behandlung von AIN II/III beschrieben, mit 50% Reduktion des Wiederauftretens nach vorheriger HPV-Impfung (Swedish, CID 2012).
