Inhalative Aspergillus-Prophylaxe bei Neutropenie
Im Falle einer Bactrim-Unvertraeglichkeit ist fuer die PCP-Prophylaxe bei HIV-Patienten die Pentamidin-Inhalation eine bewaehrte Alternative. Werden bald auch Neutropenie-Patienten prophylaktisch inhalieren – mit liposomalem Amphothericin B gegen Aspergillus?
In der CID-Ausgabe vom 01.05.2008 stellt eine niederländische Arbeitsgruppe eine randomisierte, Placebo-kontrollierte single-center-Studie vor, welche die Wirksamkeit und Verträglichkeit von inhaliertem liposomalen Amphotericin B (Ampho B) zur Prophylaxe einer invasiven pulmonalen Aspergillose (IPA) bei Patienten mit prolongierter Neutropenie untersucht hat. Die Ablagerung von Konidien (Pilzsporen) in der Lunge stellt den 1. Schritt in der Entwicklung einer IPA dar. Somit war die Hypothese, dass eine Inhalation von liposomalem Ampho B die IPA verhindern kann, möglicherweise ohne das Auftreten systemischer Nebenwirkungen.
Eingeschlossen wurden im Erasmus Medical Center in Rotterdam hospitalisierte, erwachsene Patienten mit einer hämatologischen Grunderkrankung und einer Chemotherapie-induzierten Neutropenie von mindestens 10 Tagen Dauer (Lebenserwartung mind. 3 Monate).
Von Einschluss bis zum Wiederansteigen der Neutrophilenzahl auf >300/mm3 erfolgte an jeweils 2 aufeinanderfolgenden Tagen pro Woche eine 30minütige Inhalation entweder mit Placebo oder mit 2,5ml einer 5mg/ml-Lösung liposomalen Ampho B (Chemotherapie-Beginn innert 7 Tagen nach Einschluss, max. 12 Inhalationen pro Neutropenie-Episode). Der verwendete Vernebler gab das Aerosol nur in der Inspirationsphase ab und produzierte eine durchschnittliche Partikelgrösse von 1,9um Durchmesser, was eine optimale Ablagerung in den peripheren Lungenabschnitten garantieren sollte. Die Patienten wurden nur einmal randomisiert. Das heisst Patienten in der liposomalen Ampho B-Gruppe inhalierten auch bei allfälligen weiteren Neutropenie-Episoden wieder mit liposomalem Ampho-B, Patienten in der Placebo-Gruppe analog dazu wieder mit Placebo.
Wurde gemäss EORTC-MSG-Definition (radiologisches und mykologisches Kriterium, z.B. Aspergillus-Kultur in BAL oder Galactomannan positiv in BAL bzw. Serum) eine IAP diagnostiziert (primärer Endpunkt), bedeutete dies für den Patienten das Studienende. Alle eingeschlossenen Patienten erhielten eine Fluconazol-Prophylaxe (gegen Aspergillus unwirksam). Ein HR-CT-Thorax erfolgte bei abnormem Röntgen-Thorax-Befund bzw. an Tag 5 von unklarem Fieber trotz Antibiotika-Therapie. Bei >6 Tage andauerndem unklaren Fieber in Neutropenie wurde gemäss Klinik-Standards empirisch mit Ampho B i.v. begonnen. Galactomannan wurde routinemässig im Serum (2x wöchentlich) sowie in der BAL-Flüssigkeit bestimmt.
Das Follow-up endete 28 Tage nachdem sich die letzte Chemotherapie-induzierte Neutropenie wieder auf Werte >300/mm3 erholt hatte. Für Patienten mit IPA wurd die IPA-bezogene Mortalität bis 24 Wochen nach der letzten Inhalation registriert.
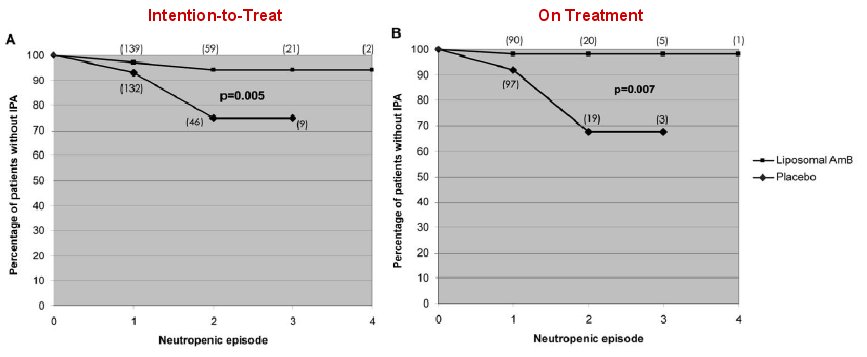
Von November 2000 bis Februar 2006 wurden 271 Patienten eingeschlossen und während 407 Neutropenie-Episoden beobachtet. Bei 339 Neutropenie-Episoden erfolgte eine Inhalationstherapie, wobei 139 Patienten (177 Episoden) liposomales Ampho B und 132 Patienten (162 Episoden) Placebo erhielten. Die beiden Gruppen wiesen bzgl. klinischer und hämotologischer Charakteristika keine signifikanten Unterschiede auf. Die Intention-to-Treat-Analyse ergab, dass 18 von 132 Patienten (14%) in der Placebo-Gruppe, aber nur 6 von 139 Patienten (4%) in der liposomalen Ampho B-Gruppe eine IPA entwickelten (p=0,005; OR 0,26 (95% CI: 0,09-0,72). Bei der On-Treatment-Analyse war der Unterschied mit einer OR von 0,14 (95% CI: 0,02-0,66) sogar noch etwas deutlicher (13/97 in der Placebo- und 2/91 in der liposomalen Ampho B-Gruppe entwickelten eine IPA). Wurden die IPA-Diagnosekriterien insofern angepasst, als dass auch ein alleiniger typischer radiologischer Befund (halo-sign oder air-crescent sign) ohne zusätzliches mykologisches Kriterium als diagnostisch galt, blieb der signifikante Vorteil der liposomalen Ampho-B-Gruppe bestehen.
In der Intention-to-Treat-Analyse zeigte sich bzgl. IPA-bezogener Mortalität zwischen Placebo (4,5% (6/132)) und liposomalem Ampho B (3,6% (5/139) kein signifikanter Unterschied (p=0.8), wohingegen in der On-Treatment-Analyse zumindest eine Tendenz zu einem Überlebensvorteil bei Inhalation mit liposomalem Ampho B zu erkennen war (IPA-bezogene Mortalität: 6,2% (6/97) mit Placebo versus 1,1% (1/90) mit liposomalem Ampho B, p=0,1).
Die Therapie-Abbruch- bzw. -Unterbruch-Rate war in der Behandlungsgruppe signifkant höher als in der Placebo-Gruppe (45 versus 30%, p=0,01). Wesentliche Nebenwirkung der Inhalation mit liposomalen Ampho B war Husten (16 versus 1 Pat. in der Placebo-Gruppe, p=0,002). Ein Anstieg des Serum-Kreatinin-Wertes wurde hingegen nicht beobachtet.
Zusammenfassung:
Bei Hochrisiko-Patienten mit prolongierter Chemotherapie-induzierter Neutropenie kann durch prophylaktische Inhalation mit liposomalem Amphotericin B die Inzidenz der invasiven pulmonalen Aspergillose signifikant reduziert werden, bei abgesehen von vermehrtem Husten guter Verträglichkeit (infolge fehlender Resorption keine systemischen Nebenwirkungen, insbesondere kein Kreatinin-Anstieg und keine Medikamenten-Interaktionen via CYP 450).
Warum also nicht das Übel bei der Wurzel packen und die in der Lunge eintreffenden Pilzsporen direkt vor Ort bekämpfen – vielleicht eine Alternative zur mancherorts eingesetzten systemischen Posaconazol-Prophylaxe?
Ausblick und Diskussion:
- Ergebnisse von Tierversuchen an Ratten deuten darauf hin, dass zur Prophylaxe eventuell auch längere Dosisintervalle ausreichen (z.B. alle 6 Wochen) (Ruijgrok et al., J Pharm Pharmacol 2005;57:1289-95) und bei der Therapie der IAP die Kombination aus Inhalation und systemischer Gabe von Amphotericin B der alleinigen i.v.-Gabe überlegen ist (Ruijgrok et al., Antimicrob Agents Chemother 2006;50:1852-4).
- Während Ampho B-Deoxycholat die Oberflächenspannung-herabsetzende Funktion des pulmonalen Surfactants stört, enthält das liposomale Ampho B Phospholipide und Cholesterol, die eine Surfactant-artige Funktion ausüben (Ruijgrok et al., JAC 2001;48:89-95).
- Ob eine Aspergillus-Prophylaxe überhaupt sinnvoll ist, hängt von der Prävalenz der IAP in der jeweiligen Patienten-Population ab (evtl. cut-off bei >10%?, Perfect, Am J Med 1993;94:233-4).
- Ampho B gehört zu den Polyenen. Im Gegensatz zu den Azolen ist die Polyen-Resistenzrate bei Pilzen sehr niedrig. Zudem sollte die hohe Konzentration von inhaliertem Ampho B in den Atemwegen einer Selektion resistenter Stämme entgegenwirken.
Links:
EORTC-MSG (Euorpean Organization for Research and the Treatment of Cancer-Mycoses Study Group)-Definition der Invasiven Pulmonalen Aspergillose: Ascioglu et al., CID 2002;34:7-14
Quelle: Rijnders, CID 2008;46:1401-08